一酸化窒素誘導体は、
①ニトロシル・ニトロソ化合物群(ままで存在)
②オキシムに異性化する化合物群
③分解群
三群に分かれる基準とは? 私の把握法は、異性化群と分解群は同類で実質二群。分解は異性化した構造が更なる安定化に向うと捉える。では二群に分かれる基準とは? その基準は既述の架空酸素分子である。一つだけが共有電子対なので架空酸素分子より電子対間の反発は弱い。しかし置換基の電気陰性度の値が小さければ共有電子対の電子がN側に偏る。つまり隣の孤立電子対との距離が短くなり、反発力が大きくなる。クーロン力は双方の電荷の積に比例し距離の二乗に反比例するからだ。下図のRとR’の結合軸で誇張的に図示した。ニロシル・ニトロソ化合物群の安定度の基準は、共有電子対が反発力でどれだけ孤立電子対に近づくか、である。

私の調べではハロゲンの誘導体の安定度:F>Cl>Br>Iとなって矛盾は無い。なおα水素の有無で分かれる原因は、α位に水素の有る方が転位・分解を起こすための活性化エネルギーが小さいからだ。これに関連することは二酸化窒素の項でも話す。
α水素が無い脂肪族三級炭素誘導体や芳香族誘導体では溶液状態では二量体との間で平衡状態とされる。二量体の化学構造を下図の右側とすると、以下のように言える。ニトロソのモノマーではCの電気陰性度の値はNより小さい。従ってC-N結合の電子対はN側に偏ることでN,Oの孤立電子対との反発が大きくなり安定化できない。
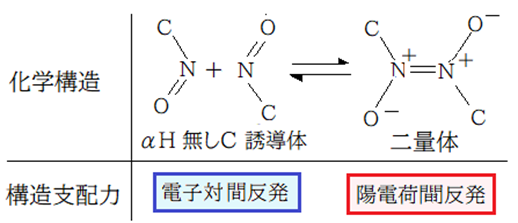
二量体ではNとOの孤立電子対間の反発は解消される。しかしNが電子対を供給する配位結合をしているのでN-N間で陽と陽の反発が発生する。Cが芳香族ならπ電子との共鳴でNの陽電荷量を減らせるが、その分Oの陰電荷とのイオン結合力が弱くなる。二量体に変ることでは安定化は実現しないのだ。
