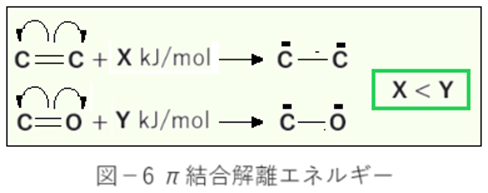
理由の一つはπ結合エネルギーだ。一酸化炭素・キノンの場合はカルボニル(C=O)のπ結合を解消することで一電子を受容する。しかしテトラシアノエチレンの場合はエチレン(C=C)のπ結合の解消だ。カルボニルのπ,σの両結合は分極によるイオン結合が加わる分結合エネルギーが大きく(図-6)なる。この結合解離エネルギーは電子親和力に対してはマイナスに働くので、C=OよりC=Cの方が有利となる。・・・①
二つ目は隣接原子の原子軌道間酸・塩基相互作用による安定化力」だ。これはカルボアニオン直結酸素ラジカル(C・――O・)が「超」大で、カルボアニオン直結炭素ラジカル(C・――C・)を大きく上回る。従ってC=CよりC=Oの方が有利となりテトラシアノエチレン電子親和力への寄与は小さい。・・・②
三つ目は一電子受容が実現した場合に付属して起こる現象だ。キノンの場合は6π電子系と隣接原子の原子軌道間酸・塩基相互作用が実現し前述の「一石二鳥」が実現する。これに対してテトラシアノエチレン(3)の場合は「陰と陽は交互」が実現(Ⅱ-5参照 / 図-7)する。図-7には記してないが陰・陰による斥力はテトラシアノエチレン(3)・テトラシアノエチレンラジカルアニオン(3--)共にゼロである。しかし3では陽・陽の反発結合部位が5個あることで電子を呼び込み易くなっている。3が電子一つ取り込むだけで陽・陽反発状態の結合が5個全て消滅し、「陰と陽が交互」による安定化の「場」が4個から8個に増える。・・・③
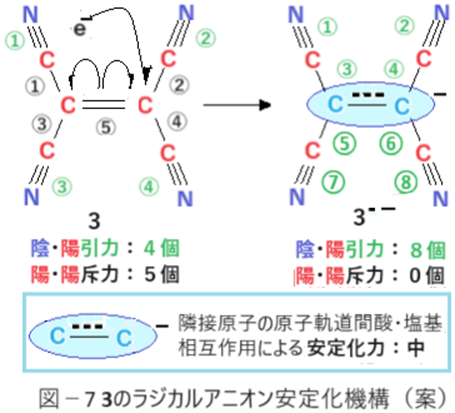
テトラシアノエチレン安定化貢献度を100%私の主観で表せば、③≧①≫②となる。テトラシアノエチレン(3)の大きな電子親和力の原因は、カルボニルを壊すほどの大きなエネルギー損失が無く、陰と陽が交互による安定化が分子全体で実現することだ。隣接原子の原子軌道間の酸・塩基相互作用による安定化力は小さく大きな寄与はない。
どうして電子は三重結合で陽電荷(量)も多いニトリルのC原子ではなくエチレンのCに? の疑問には以下の答えを用意しています。一言で言えば、ベンゾキノン(Ⅳ-3)と同様に「速やかな安定型への移行」と捉えます。
仮にニトリルのC原子に一電子受容した3‘ラジカルアニオン(3‘・- / (図-8)では「陰と陽は交互」が分子全体で実現しない。カルボアニオン直結Nラジカル(C・――N・)は、カルボアニオン直結Cラジカル(C・――C・)より安定化力が大きいが一つのCNでしか実現しない。前述のようにエチレンのCが一電子受容すれば「陰と陽は交互」が分子全体で実現する故にC=Cに電子を受容した方がエネルギー的に有利だ。仮にCNのCに電子を受容しても図-8の黒の細線で囲った部分で表したようにCの電子対とNの孤立電子の玉突き様移動でより安定な緑線で囲った3ラジカルアニオン(3・-)へ変化すると解釈。

